El ácido desoxirribonucléico ó ADN es una molécula de tipo polímero ya que está compuesta por una cadena de monómeros unidos entre sí. Cada monómero se llama nucleótido, que a su vez está constituído por tres componentes: una base nitrogenada, una pentosa (azúcar de cinco carbonos) y un fosfato.
La base del código genético la dictan las bases nitrogenadas. Son cuatro en el ADN Adenina y Guanina (A y G), que son bases púricas y Citosina y Timina (C y T), que son bases pirimidínicas. En el ARN la Timina deja lugar a la base llamada Uracilo (U). Por lo tanto existen cinco tipos de bases nitrogenadas. La combinación de las bases nitrogenadas provoca la generación del código genético. Por eso se pueden ver que las secuencias de ADN son del tipo “AACTGGGTCATGCGAA”.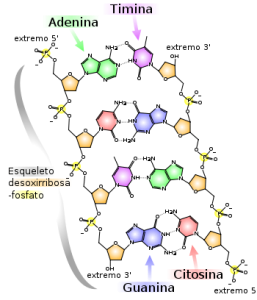
Hasta ahora se ha hablado de la formación de una hebra de ADN. Pero la forma básica de nuestro material hereditario no se encuentra un una sola hebra. Dos de estas hebras, que son complementarias por las uniones entre las bases púricas y las pirimidínicas (A con T y C con G), forman la doble hélice de ADN. Tiene un tamaño de 20 Armtrongs de diámetro y da una vuelta completa cada 34 Armstrongs. 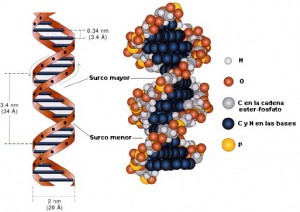
Bueno, espero que haya sido de utilidad. Si tenéis dudas, comentadlas e intentaré aclararlas todas.
Ciencia
Aquí encontrarás todo lo relacionado con la ciencia y su divulgación. Gran parte, desarrollado de la extinta web "Blog de laboratorio".
Editar y fusionar PDFs
Cuando se trabajan con varios artículos y se quiere tener un archivo limpio, la duda de cómo lograr un pdf a la carta surge al instante. En todas las plataformas se puede hacer fácilmente con la versión Pro del Adobe Reader. Sin embargo, no está el bolsillo para adquirir licencias. Los usuarios de Mac OS lo tenemos fácil. Tan solo hay que abrir el archivo pdf con Vista previa y empezar a editar. Se pueden quitar páginas dando símplemente a eliminar seleccionando las que se quiera quitar. También se pueden añadir más páginas arrastrándolas a la posición deseada en la barra lateral. Permite así fusionar pdfs y hacerlos a medida. Para guardar el archivo final, tan sólo hay que seleccionar todas las páginas, ir a “Archivo” y después seleccionar “imprimir”. En el diálogo se puede ver el botón “PDF” y seguidamente “guardar como pdf”. Sólo hay que rellenar los campos necesarios para guardarlo y listo. Os dejo un vídeo hecho por mí para que veais lo simple que es:
[youtube]http://www.youtube.com/watch?v=8l-sdnsp6Ig[/youtube]
Manipulación de muestras de ADN
A la hora del manejo de las muestras de ADN hay que tener varios factores en cuenta: primero la esterilidad y pureza del lugar donde se depositan. Evidentemente las muestras de ADN no se almacenan en un tubo cualquiera. El vial destinado para ello debe ser estéril y haber sido autoclavado previamente. Parece una redundancia, pero no es así. Los viales vienen de las empresas comercializadoras con un certificado de esterilidad. En un laboratorio suele haber un grupo amplio de investigadores. Cada uno con sus manías y sus protocolos de esterilización. Lo usual es que se repartan viales en otros recipientes para que cada uno tenga su material. Y esos contenedores deben ser de un material, como el vidrio, que resista altas temperaturas. De este modo no hay que preocuparse tampoco de cómo han sido rellenados los recipientes con los viales ya que, antes de pasar al investigador, son autoclavados: esterilizados mediante la acción de vapor de agua a cierta presión durante un tiempo determinado.
Así también pasan por el mismo proceso todos los materiales desechables que se utilicen como puntas de micropipetas, tubos de ensayo, probetas u otros recipientes y viales.
Algo que no he comentado es la situación del personal del laboratorio. Se deben usar guantes en todo momento. Esto es debido a que en las manos tenemos unas enzimas llamadas DNAsas que digieren el ADN. El simple contacto de los viales y/o las muestras con las DNAsas sería fatal. Otra precaución que se toma siempre es mantener las muestras en frío siempre y cuando los protocolos de manipulación no indiquen lo contrario. El recipiente de poliestireno relleno de hielo picado es otro compañero más en el laboratorio.
Dependiendo del tipo de muestras y del nivel de purificación que se necesite para su procesado y estudios posteriores, hay que almacenar el ADN diluído desde simple Agua estéril y filtrada (Agua MiliQ) hasta en buffers (soluciones tamponadas) específicos que permitan una mayor eficiencia en el análisis. También puede que necesiten seguir algún protocolo de purificación mediante técnicas tradicionales o con kit especiales para ello.
Por último, el almacenamiento de las muestras debe realizarse a 4ºC si se van a utilizar en periodos de tiempo medio (unas semanas) o a -20ºC si se piensa almacenar para análisis no a corto plazo. Nunca se deben congelar y descongelar muy sucesivamente las muestras porque los cristales de hielo formados en la congelación pueden romper las hebras de ADN, empeorando rendimientos.
Seguiré con más lecciones de laboratorio pronto.
Escuchando:
Melonomics
La secuenciación del genoma del melón es uno de los proyectos más ambiciosos de los grupos de investigación financiado por Genoma España.  Ya se tiene un borrador de todo el genoma que tiene un tamaño aproximado de 450 millones de pares de bases en sus 12 cromosomas, con un total de 26.000 genes. Además de la secuenciación de una línea de melón, MELONOMICS pretende caracterizar un gran número de variedades de esta especie presentes en los bancos de semillas españoles.
Ya se tiene un borrador de todo el genoma que tiene un tamaño aproximado de 450 millones de pares de bases en sus 12 cromosomas, con un total de 26.000 genes. Además de la secuenciación de una línea de melón, MELONOMICS pretende caracterizar un gran número de variedades de esta especie presentes en los bancos de semillas españoles.
En diversos congresos a los que he asistido, se mostraron resultados previos de estos estudios y eran más que prometedores. No olvidemos que el melón tienen un gran valor económico ya que somos los primeros exportadores de este fruto.
Fuente: SINC
Tomorregulina, ¿represor tumoral?
Se están abriendo nuevos campos en el estudio del cáncer. La universidad de Santiago de Compostela y gracias al grupo liderado por Anxo Vidal Figueroa, ha estudiado esta proteína. La tomorregulina (Tmeff2), una proteína transmembrana que es segregada como hormona, encuentra disminuida su expresión en diferentes tipos tumorales, como el cáncer colorrectal, uno de los que provoca mayor mortalidad después del cáncer de pulmón. Se descubrió que la proteína se vuelve inactiva en los estadios iniciales del cáncer.
Por ahora el estudio se encuentra en análisis preclínicos observando la acción de la sobreexpresión del gen en ratones transgénicos.
Fuente: USC
Extracción de ADN
Lo más habitual en cualquier laboratorio de genética es extraer el ADN de cualquier tejido o superficie. En mi caso he podido extraer ADN de hojas de plantas, de semillas, de tejido de lagarto, de lodo, de sangre…e incluso de los compuestos obtenidos de un tanque de fermentación.
Hace unos años era necesario preparar para cada ocasión una serie de tampones o buffers para poder extraer el material hereditario. Y cada disolución tenía que prepararla cada uno. Ahora todo es muy sencillo. Existen kits de extracción para cada tipo de tejido o muestra a analizar. La utilización de estos kits tienen sus pros y sus contras: generalmente la eficiencia de la extracción (la cantidad de ADN obtenido por extracción) suele ser bastante mayor con los métodos tradicionales. Sin embargo, la pureza del ADN aislado es mayor cuando se usan los kits. Dependiendo para qué se vaya a utilizar el ADN y el tipo de estudio, será mejor tener más ADN y menos puro ó viceversa. Las nuevas tecnologías suelen “funcionar” mejor cuanto más limpia sea la extracción, ya que en muchas ocasiones recomiendan purificarlo.
Cuando ya se tiene el vial con el ADN disuelto en el tampón de elución, siempre hay que hacer una cuantificación. Con aparatos como el NanoDrop, la cantidad de ADN utilizado para cuantificar es de tan sólo 1 microlitro. Para hacerse una idea, es poco más de lo que ocupa la impresión del punto en el teclado de un ordenador. Hay ocasiones en que existen problemas con las mediciones y se opta por seguir el método tradicional que consiste en hacer un gel de agarosa a una concentración del 0,8% y realizar una electroforesis de todas las extracciones. Posteriormente, la imagen que se obtiene en el transiluminador de rayos ultravioleta (siempre que se utilicen marcajes como el bromuro de etidio o SybrGreen) se utiliza para hacer un cálculo estimado de la concentración de ADN gracias a la extrapolación que nos permite el marcador de fragmentos de ADN (un marcador de ADN en escalera (DNA ladder) no es más que un fragmento de ADN el cuál ha sido cortado de forma que se obtienen bandas de un tamaño conocido), ya que sí que sabremos la concentración cargada en el gel de ese marcador.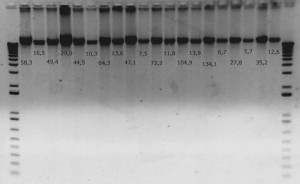
Escuchando: canciones en Jamendo.com
